Et holistisk syn på organismen og dens mikroorganismer
Meget tyder på, at samspillet mellem en værtsorganisme og dens mikrober er enorm vigtigt for både værten og dens mikrobers udvikling. Denne erkendelse kan betyde, at vi skal til at omskrive og nytænke alt fra evolution til fødevareproduktion.
Af Thomas Sten Pedersen, Christina Lehmkuhl Noer og Morten Tønsberg Limborg
Mere og mere tyder på, at vores eksistens medbestemmes af de mikrober, vi omgives af – altså de milliarder af mikroorganismer, der er i os, på os, og overalt omkring os. Det første mikrobiske liv er dateret til mere end 3,5 milliarder år siden, og er dermed omkring 3 milliarder år ældre end de første flercellede organismer. Med andre ord betyder det altså, at vi og alle andre flercellede organismer er udviklet i en verden, som mikrober har skabt. Derfor er det heller ikke overraskende at forskning, som dykker ned i samspillet mellem en værtsorganisme og dens milliarder af tilhørende mikrober finder, at disse mikrober har enorm betydning for organismers udvikling og helbred.
Dette samspil mellem værtsorganismer og deres mikrober er netop, hvad forskere indenfor det nye forskningsfelt hologenomics undersøger. I hologenomics anser man værten og dens tilhørende mikrober som én samlet organisme. Mikrober såsom virus, bakterier, mikroskopiske svampe og andre typisk encellede organismer bærer dermed en del af ansvaret for, hvorfor organismer udvikler sig, som de gør. Tesen er, at værten og dets mikrober er i konstant samspil, hvilket afgør, hvordan værten opfører og udvikler sig. Med andre ord påvirker værten sine mikrober, mens mikroberne “skubber” tilbage og påvirker værten på et væld af forskellige måder. Ændringer i mikrobernes sammensætning vil dermed blive oversat til ændringer i værtsorganismen. Disse ændringer spænder lige fra sundhed til adfærd til udseende.
Som udtrykket antyder, er hologenomics et holistisk perspektiv, der sikrer, at forskningen ikke kun fokuserer på separate faktorer såsom miljø eller genetik, men i stedet sporer forskningen hen imod et bredt helhedsbillede af en værtsorganisme og dets mikrober. Hologenomics er i den forstand et værktøj, man kan bruge til bedre at forstå mikrobernes betydning for deres vært gennem genetik, og værtens genetik gennem mikrobiomet.
Mikrobiomet i fokus
Et mikrobiom er den samlede masse af mikrober, som lever på, i og omkring en værtsorganisme. Taler man om det menneskelige mikrobiom, medregner man derfor alle de milliarder af bakterier, vira, mikroskopiske svampe og andre typisk encellede organismer, som lever i, på og til dels også omkring mennesket. Mikrobernes samlede arvemateriale (metagenomet) kan ses som en forlængelse af værtsorganismens egen arvemasse – dets såkaldte genom – men værtsorganismens miljø og adfærd påvirker også dets sammensætning af mikrober.
Genomet koder for de proteiner, der udgør værtens væv. Det vil sige, at den måde genetikken gør, at vi mennesker ser forskellige ud også gør sig gældende indvendigt eksempelvis på overfladen af tarmen. Så når vi er genetisk forskellige, er vores tarmes mikrobiomer også forskellige. Det betyder, at der er individuel forskel på, hvilke bakterier som trives i vores tarme, og hvilke der ikke gør.
Taler man om et mikrobiom, taler man derfor om en levende, individuel og dynamisk masse, som med hologenomiske øjne bør anses som afgørende for værtens udvikling. Netop fordi et mikrobiom både er levende og påvirker dets værts udvikling, er forskning i interaktionen med værten spændende. Forstår man, hvordan en specifik mikrobesammensætning i et mikrobiom påvirker værten, og hvorfor den gør det, kan man manipulere mikrobesammensætningen på en måde, som gavner værtsorganismen.
Hologenomics forklaret
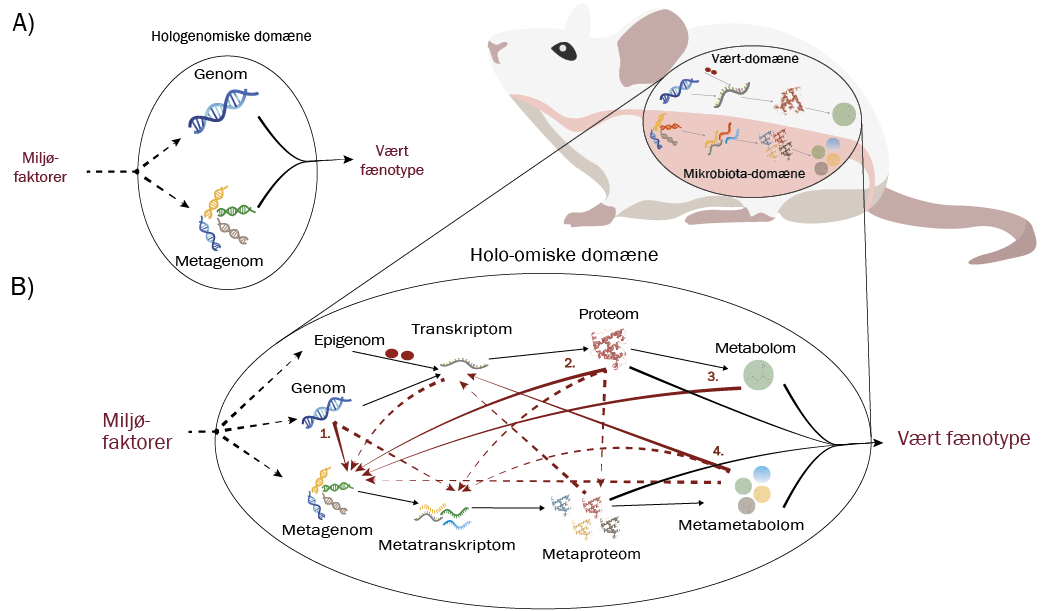
Figuren illustrerer, hvordan hologenomics undersøger både værtens arvemasse (genomet) og dens mikrobers samlede arvemateriale (metagenomet) for at kunne forudsige, hvordan disse sammen med deres miljø påvirker værtens udseende og funktionelle formåen, kaldet dens fænotype (A).
I B zoomes der ind på kompleksiteten i, hvordan værtens og dens mikrobers arvemateriale påvirker hinanden i alle led af processerne inde i værten. Denne samling af værts-mikrobe interaktioner kaldes det holo-omiske domæne. Hvis man dykker ned i figuren, viser den øverste del af cirklen de forskellige niveauer, hvorpå værten påvirkes nemlig: genomet, epigenomet, transkriptomet, proteomet og metabolomet. Nederst ses de forskellige niveauer, hvor mikroberne kan påvirkes kaldet metagenomet, metatranskriptomet og metaproteomet. Pilene på illustrationen viser interaktionerne mellem værten og dens mikrober. De mange fagtermer defineres således for værtens niveauer:
Genomet: værtsorganismens samlede arvemateriale (DNA).
Epigenomet: Kemiske modifikationer på vores DNA, som ikke ændrer selve DNA-sekvensen, men som har betydning for, hvilke gener der er aktive i cellen.
Transkriptomet: Den samlede mængde af enstrengede RNA sekvenser, som er blevet transkriperet fra værtens aktive gener og eventuelt senere oversættes til proteiner i cellen.
Proteomet: Den samlede mængde proteiner, der findes i en vævsprøve på et givet tidspunkt.
Metabolomet: Den samlede mængde metabolske molekyler i en prøve, for eksempel fedtsyrer og aminosyrer i tarmen, og som kan være syntetiseret af enzymer fra enten værtens eller mikrobernes gener. Mikrobernes niveauer defineres således:
Metagenomet: Den samlede arvemasse fra alle de mikrober, der findes i en prøve, for eksempel tarmen.
Metatranskriptomet: Den samlede mængde af enstrengede RNA-sekvenser, som er blevet transkriperet fra alle mikrobernes aktive gener og eventuelt senere oversættes til proteiner i eksempelvis tarmen.
Metaproteomet: Den samlede mængde proteiner, der findes i en vævsprøve på et givet tidspunkt, og som er lavet på baggrund af gener i mikroberne.
Mavens magt
Et af de mest betydningsfulde mikrobiomer i mennesket er tarmen, og der bliver derfor forsket rigtigt meget i tarmens mikrober. Nye studier har vist, at tarmens mikrober er med til at påvirke alt fra appetit og humør til livsstilssygdomme i mennesker, og det er tilmed lykkedes forskere at få sunde rotter til at udvise depressionstræk og frygtsom adfærd ved at transplantere afføring fra frygtsomme til sunde rotter. Det nye behandlingsfelt indenfor fæcestransplantation udnytter netop også tarmen og dens mikrobers påvirkning af mennesket til at genskabe en flora i balance, som kan have været tabt under for eksempel en skrap antibiotikakur. Desuden bliver eksempelvis 95% af signalstoffet serotonin produceret i menneskets tarmceller, hvilket påvirker søvn, appetit og sindsstemning. Tarmens mikrober er altså ikke bare med til at nedbryde den mad, du spiser. De er også med til at skabe et miljø i dine tarme, som er mere eller mindre gunstig for dig.
Maven og mikrobernes magt er altså et forskningsområde i vækst inden for flere discipliner, og har blandt andet stadig uforløst potentiale indenfor behandling og personlig medicin. Det hologenomiske perspektiv kan hjælpe med at indfri potentialet, netop fordi der genetisk tages højde for både værten og alle dens mikrober. Et menneskes mikrobiom er nemlig unikt, og det ændrer sig over et liv. Der er derfor ingen tommelfingerregel for, hvilken mikrobesammensætning der skaber balance i et menneske. Derfor skal personlig medicin eller probiotika skræddersyes til både patientens unikke genom såvel som mikrobiom for at kunne manipulere dets samspil med værten til det bedre. Det samme gælder fæcestransplantationer, som kan gøres sikrere og mere effektive, når der er så stor genetisk lighed mellem donor og patient som muligt. Kernen af det hologenomiske perspektiv, samspillet mellem en vært og dens mikrober på genetisk niveau, kan i denne forstand bruges til at forbedre den nye forskning i mavens magt over mennesket.
Akvakultur og ny hologenomisk forskning
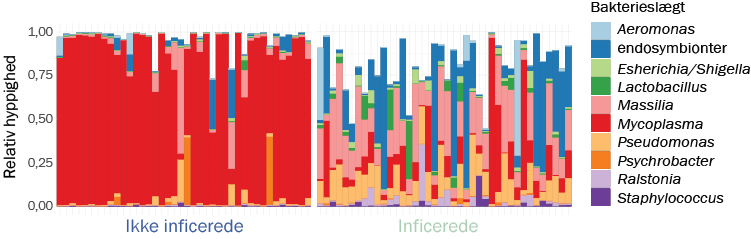
Akvakultur er den hurtigst voksende fødevareindustri lige nu, og derfor har ethvert fremskridt i bæredygtig retning enormt potentiale. Ny hologenomisk forskning har blandt andet fundet en sammenhæng mellem mangfoldigheden af Mycoplasma-bakterien og sundheden af norske opdrætslaks, samt hvor store laksene vokser sig. Dette forskningsresultat kan være svaret på et mysterium, akvakultur har døjet med siden sin begyndelse, nemlig at nogle laks vokser sig til 1 kilo, mens andre fra samme kuld, besætning og miljø vokser til sig til 10 kilo. De store laks i disse kuld har allesammen mangfoldighed af Mycoplasma i deres tarm-mikrobiom. Meget tyder derfor på, at akvakultur kan effektivisere foderbrug og mindske sygdomsudbrud i deres laksebestande, hvis de sikrer mangfoldighed af Mycoplasma i laksene, eksempelvis med probiotika. Arbejdet med at bruge hologenomics til at forbedre akvakulturs bæredygtighed er støttet af EU H2020-projektet HoloFood og Danmarks Frie Forskningsfond via projektet HappyFish. Netop HappyFish forsker i, hvordan akvakultur kan gøres mere bæredygtigt ved at anvende det hologenomiske perspektiv.

Hologenomics’ brede anvendelse
Mens mikrobiomet spiller en afgørende rolle for værtens helbred og udvikling, går hologenomics endnu dybere til værks end “blot” at se på samspillet mellem vært og mikrobiom. Det gøres ved både at analysere værtens og mikrobernes arvemasse gennem gensekventering. Man kan sige, at mikrobiomet er en måde, vi afgrænser, hvilke mikrober vi kigger på, og hologenomics er måden, hvorpå vi undersøger mikrobiomets genomer og deres indflydelse på værten. Det er altså ikke kun enkelte gener, man ser på i hologenomics, men hele arvemassen for både værtsorganismen og dets tilhørende mikrober.
Det er relativt nyt, at man overhovedet kan redegøre for både værtens og mikrobernes arvemasse. Det er blevet muliggjort af nye teknologiske landvindinger inden for DNA-sekventering og computerkraft, som gør det muligt at analysere de kæmpe mængder data, og vi er stadig kun i forskningsfeltets spæde start. Hologenomics har taget disse teknologiske landvinder i brug for at undersøge samspillet mellem vært og mikrober. Dette perspektiv åbner op for nye muligheder for at optimere og effektivisere alt fra medicin til fødevareproduktion på land og i vand.
Hologenomics og dets potentiale spænder altså bredt, og mens det potentielt kan nuancere måden, vi tænker de store strøg såsom evolution på, har det samtidig stort praktisk potentiale i flere betydningsfulde industrier som medicin og fødevareproduktion. Et praktisk eksempel på anvendelse af hologenomics er HoloFood-projektet.
En bæredygtig fødevareproduktion
HoloFood udnytter den nye viden om vært-mikrobe-forholdet til at gøre verdens fødevareproduktion mere bæredygtig. Projektet fokuserer på at optimere særligt akvakultur og fjerkræproduktion ved at tage højde for det enkelte individs mikrobersammensætning og bruge dette til at forbedre dyrenes sundhed og trivsel. Den hologenomiske tilgang gør, at man kan skræddersy fodersammensætningen med probiotika, hvilket er et fodertilskud med udvalgte mikrober, tilpasset til det enkelte dyr og dets mikrobiom.
Som eksempel har norske og chilenske laks afgørende genetiske forskelle, og derfor findes der ikke et universelt gavnligt foder eller probiotika til laks. I stedet bør foderet udvikles specifikt til den individuelle laksestamme, hvilket kan give bedre vækstresultater med mindre spild. Man kan med andre ord få flere og sundere laks for mindre foder, hvilket i stor skala kan have enorm effekt på fødevareindustriens bæredygtighed.
Rent praktisk undersøger HoloFood sammensætningen af dyrenes tarm-mikrober ved at indsamle afføringsprøver, som bliver gen-sekventeret og sammenlignet med referencer fra sunde dyr, der vokser, som de skal. På den måde bliver vært-mikrobe dataen brugt til at afgøre, hvilke probiotika man skal tilføre fodersammensætning. Foruden de bæredygtige fordele ved at effektivisere foderbrug sikrer det desuden højere grad af velfærd hos produktionsdyrene, og lader industrien sætte ind mod fejlernæring eller med medicin mod potentielle sygdomsudbrud i en besætning.
Det nye forskningsfelt hologenomics
Hologenomics er et helt nyt felt indenfor grundforskning i en værtsorganismes og dens mikroorganismers genomer. Hologenomics er måden, hvorpå vi undersøger mikrobiomets genomer og deres indflydelse på værten. Det er altså ikke kun enkelte gener, man ser på i hologenomics, men hele arvemassen for eksempelvis både mennesket og dets tilhørende mikrober.
Center for Evolutionary Hologenomics (CEH) er en del af GLOBE Instituttet på Københavns Universitet og er indtil videre det eneste forskningscenter i verden, som dykker ned i det nye hologenomics felt. Centeret åbnede i 2020 med støtte fra Danmarks Grundforskningsfond og ledes af Professor Tom Gilbert. CEH har 60 associerede forskere og ansatte, inklusiv 29 postdocs og ph.d.-studerende. Læs mere om CEH på vores hjemmeside www.ceh.ku.dk. Video om CEH her: youtu.be/4HrBTAf_xow
En fremtid med hologenomics
Den indsigt i samspillet mellem vært og mikrober, som hologenomics frembringer, kan bringes i spil i et væld af industrier. Som tidligere nævnt er det et yderst brugbart perspektiv i personlig medicin til bedre at kunne skræddersy behandling til den enkelte patient, men også som værktøj til, når man skal vælge donorer af både fæces og organer til transplantationer. Foruden mennesker og dyr forskes der desuden også i, hvordan det hologenomiske perspektiv kan bruges til at forstå og modificere planter og afgrøder til bedre at kunne modstå en fremtid med tørke og mere ekstremt vejr, som følge af klimaforandringer.
Hologenomics er stadig et ungt forskningsfelt, hvis fulde anvendte potentiale er ved at blive kortlagt og undersøgt. Allerede nu er det dog klart, at samspillet mellem værtsorganisme og dets mikrober bringer nye dimensioner til alt fra planter til mennesker og medicin, til fødevarer på land og i vand, og hvordan vi bør anskue evolution i en mikrobiel verden.